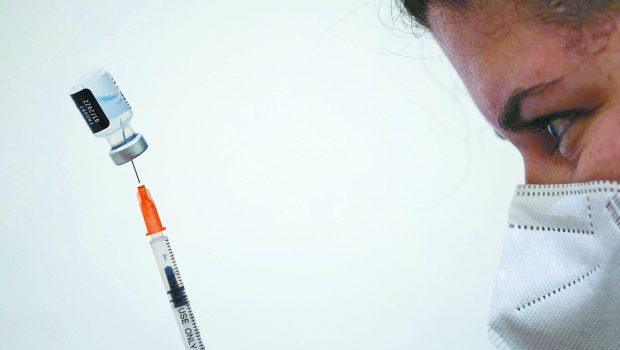
Nέες κανονιστικές οδηγίες για μελλοντικά ενισχυτικές δόσεις για τα εμβόλια Covid-19 παρουσίασε την Τρίτη ο αμερικανικός Οργανισμός Τροφίμων και Φαρμάκων (FDA), ορίζοντας αυστηρότερα πρότυπα έγκρισης για υγιείς Αμερικανούς.
Ο FDA συνέστησε διαφορετικά πρότυπα αποδεικτικών στοιχείων για την έγκριση με βάση τον κίνδυνο των ασθενών να αρρωστήσουν σοβαρά από Covid, σύμφωνα με άρθρο που δημοσιεύθηκε την Τρίτη στο New England Journal of Medicine. Οι συγγραφείς του άρθρου είναι ο Επίτροπος του FDA, Marty Makary, και ο Vinay Prasad, ένας σφοδρός επικριτής της φαρμακευτικής βιομηχανίας, ο οποίος διορίστηκε επικεφαλής του τμήματος του οργανισμού που επιβλέπει τα εμβόλια.
Οι νέες οδηγίες έρχονται καθώς ο Υπουργός Υγείας και Ανθρωπίνων Υπηρεσιών, Ρόμπερτ Φ. Κένεντι Τζούνιορ, ένας φανατικός «πολέμιος» των εμβολίων, αναθεωρεί τις υπηρεσίες υγείας της χώρας.
Για ενήλικες 65 ετών και άνω, και για άτομα ηλικίας μόλις 6 μηνών που έχουν ορισμένα υποκείμενα νοσήματα, ο FDA δήλωσε ότι θα αποδεχτεί τα δεδομένα ανοσογονικότητας – τα οποία δείχνουν ότι ένα εμβόλιο προκαλεί μια αρκετά ισχυρή απόκριση αντισωμάτων – ως επαρκή για να διαπιστωθεί ότι τα οφέλη μιας ένεσης υπερτερούν των κινδύνων της.
Tι αλλάζει ο FDA για τα εμβόλια από υγιή άτομα
Αλλά για υγιή άτομα ηλικίας μεταξύ 6 μηνών και 64 ετών που δεν έχουν παράγοντες κινδύνου, ο οργανισμός σχεδιάζει να απαιτήσει ισχυρότερα στοιχεία για τα εμβόλια από τυχαιοποιημένες, ελεγχόμενες δοκιμές. Αυτές οι μελέτες πρέπει να δείχνουν πραγματικά κλινικά αποτελέσματα, όπως λιγότερες μολύνσεις ή νοσηλείες, πριν ο FDA χορηγήσει πλήρη έγκριση για ένα εμβόλιο.
Κατά την έγκριση ενός εμβολίου Covid για άτομα υψηλού κινδύνου, ο FDA θα ενθαρρύνει τους κατασκευαστές να διεξάγουν τυχαιοποιημένες, ελεγχόμενες κλινικές δοκιμές σε υγιείς ενήλικες στο πλαίσιο της δέσμευσής τους μετά την κυκλοφορία του εμβολίου στην αγορά.
Προηγουμένως, ο FDA βασιζόταν περισσότερο σε δεδομένα ανοσογονικότητας κατά την αξιολόγηση των ενισχυτικών εμβολίων Covid – τα οποία είναι προσαρμοσμένα σε νέα στελέχη του ιού που κυκλοφορούν – για έγκριση για όλους τους Αμερικανούς κάθε χρόνο. Αυτή η προσέγγιση αντικατόπτριζε το μοντέλο του εμβολίου της γρίπης, όπου οι ετήσιες ενημερώσεις στελεχών εγκρίνονται με βάση τα δεδομένα ανοσολογικής απόκρισης, όχι τις πλήρεις κλινικές δοκιμές.
«Η νέα φιλοσοφία του FDA για την Covid-19 αντιπροσωπεύει μια ισορροπία μεταξύ κανονιστικής ευελιξίας και δέσμευσης στην επιστήμη των “χρυσών προτύπων”», ανέφερε ο οργανισμός σε ανακοίνωσή του. «Ο FDA θα εγκρίνει εμβόλια για άτομα υψηλού κινδύνου και, ταυτόχρονα, θα απαιτήσει ισχυρά, “χρυσού προτύπου” δεδομένα για άτομα χαμηλού κινδύνου».
Πηγή: ot.gr
Πηγή: in.gr